Фолієва кислота необхідна для здоров'я вагітних жінок і їх плоду. Глюкозамінова сіль (6S)-5-метилтетрагідрофолату як активна форма фолієвої кислоти була схвалена для використання в кількох регіонах.
Однак Міністерство охорони здоров’я Бразилії та Національне агентство з нагляду за здоров’ям (ANVISA) нещодавно випустили особливе попередження про ризик використання (6S)-5-метилтетрагідрофолату глюкозамінової солі вагітними жінками, що привернуло увагу промисловості та призвело до дискусій. .
Ключові пункти попередження від Міністерства охорони здоров’я Бразилії та Національного агентства з нагляду за здоров’ям (ANVISA):
Міністерство охорони здоров’я та ANVISA, після ретельного аналізу поточних наукових досліджень і з твердою прихильністю громадському здоров’ю, спеціально відзначили, що вагітні жінки повинні брати до уваги обмеження поточних наукових досліджень і оцінювати свій особистий стан здоров’я, розглядаючи можливість використання препарату. глюкозамінової солі (6S)-5-метилтетрагідрофолату. Ця ініціатива покликана забезпечити безпеку вагітних жінок та їхніх плодів, а також застерегти споживачів і медичних працівників від ретельної оцінки таких продуктів, перш ніж зробити вибір.
Огляд і оновлення історичних регуляторних директив:
У 2018 році ANVISA випустила регуляторну директиву № 28, яка вперше розглядає ризики, пов’язані з використанням певних добавок фолієвої кислоти вагітними жінками. Директива вимагає, щоб на етикетках продуктів було чітко зазначено:
«Попередження «У вагітних жінок необхідно оцінити, чи виправдовує стан матері потенційний ризик для плоду, враховуючи (6S)-5-метилтетрагідрофолат глюкозамін, оскільки докази дуже обмежені для визначення ризику цієї сполуки під час вагітності. ' має бути зазначено на маркуванні продукту».


Регуляторне посилання: http://antigo.anvisa.gov.br/documents/10181/3898888/An%C3%A1lise+de+Contribui%C3%A7%C3%B5es+-+Ciclo+Discuss%C3%A3o+-+Suplementos +Alimentares/d3c135a6-6560-4f33-8c2d-09f29434bd34?version=1.0
У 2020 році ANVISA випустила нормативну директиву № 76, яка підтверджує вміст попереджень на етикетках продуктів, щоб переконатися, що споживачі отримують чітку інформацію та можуть зважити ризики використання.
«Попередження «У вагітних жінок необхідно оцінити, чи виправдовує стан матері потенційний ризик для плоду, враховуючи (6S)-5-метилтетрагідрофолат глюкозамін, оскільки докази дуже обмежені для визначення ризику цієї сполуки під час вагітності. ' має бути зазначено на маркуванні продукту».


Регуляторне посилання: http://antigo.anvisa.gov.br/documents/10181/5809185/IN_76_2020_.pdf/dfd37f9a-678f-4d04-86e7-d44a8ee9490b
Висновок:
Захід, вжитий Бразилією, не тільки служить гарантією для її споживачів, але й створює важливий прецедент для використання фолієвих добавок у всьому світі. У ньому підкреслюється, що різні регіони можуть мати різні рекомендації щодо одного продукту через відмінності в регуляторній політиці, еволюції наукових досліджень і різноманітних потреб громадського здоров’я. Це служить нагадуванням про те, що при виборі та використанні будь-якої харчової добавки важливо враховувати регіональні відмінності та дотримуватися вказівок місцевих регуляторних органів.
Цей звіт має на меті передати попередження про ризик, видане Міністерством охорони здоров’я Бразилії та ANVISA щодо використання (6S)-5-метилтетрагідрофолату глюкозамінової солі вагітними жінками. Надана інформація лише для довідкових цілей, а для отримання додаткової інформації відвідайте офіційний веб-сайт ANVISA за адресою anvisa.gov.br.

 Español
Español Português
Português  русский
русский  Français
Français  日本語
日本語  Deutsch
Deutsch  tiếng Việt
tiếng Việt  Italiano
Italiano  Nederlands
Nederlands  ภาษาไทย
ภาษาไทย  Polski
Polski  한국어
한국어  Svenska
Svenska  magyar
magyar  Malay
Malay  বাংলা ভাষার
বাংলা ভাষার  Dansk
Dansk  Suomi
Suomi  हिन्दी
हिन्दी  Pilipino
Pilipino  Türkçe
Türkçe  Gaeilge
Gaeilge 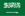 العربية
العربية  Indonesia
Indonesia  Norsk
Norsk  تمل
تمل  český
český  ελληνικά
ελληνικά  український
український  Javanese
Javanese  فارسی
فارسی  தமிழ்
தமிழ்  తెలుగు
తెలుగు  नेपाली
नेपाली  Burmese
Burmese  български
български  ລາວ
ລາວ  Latine
Latine  Қазақша
Қазақша  Euskal
Euskal  Azərbaycan
Azərbaycan  Slovenský jazyk
Slovenský jazyk  Македонски
Македонски  Lietuvos
Lietuvos  Eesti Keel
Eesti Keel  Română
Română  Slovenski
Slovenski  मराठी
मराठी  Srpski језик
Srpski језик 






 Online Service
Online Service