Органи охорони здоров'я Північної Америки рекомендують 0,4 мг фолієвої кислоти на день до зачаття
протягом всієї вагітності, щоб зменшити ризик дефектів нервової трубки. Як зазвичай, є фолієва кислота та L-метилфолат для вагітних.
Чи натуральна (6S)-5-метилтетрагідрофолієва кислота така ж ефективна, як синтетична фолієва кислота, щодо підвищення концентрації фолату в сироватці крові та еритроцитах під час вагітності?
У 2020 році в статті, опублікованій у «BMC (Part of Springer Nature)», було зазначено, що добавки (6S)-5-метилтетрагідрофолієвої кислоти настільки ж ефективні, як і синтетична фолієва кислота, у підвищенні концентрації фолату в сироватці крові та еритроцитів під час вагітності, водночас знижуючи рівень УМФА. Ця стаття підтвердила, що високе споживання фолієвої кислоти викликає занепокоєння, оскільки виявляється, що активність DHFR обмежена, а метаболічні ефекти неметаболізованої фолієвої кислоти (UMFA) невідомі. Наявність UMFA у грудному молоці викликає занепокоєння, оскільки вона може погіршити біодоступність фолієвої кислоти в молоці. Фолієзв'язуючий білок (FBP) у грудному молоці має вищу спорідненість до фолієвої кислоти, ніж її відновлені форми; після проковтування фолієва кислота може менш легко вивільнятися FBP, коли вона проходить через шлунково-кишковий тракт, зменшуючи подальше всмоктування та потенційно впливаючи на немовля’фолієвий статус.
Щоб вирішити проблему UMFA для людей із проблемою MTHFR , Jinkang Pharmaceutical Technology розробила MEGNAFOLATE®, запатентованийбіологічно активний фолат, вітамін B9 (5-MTHF) . це чистіше, безпечніше та легше засвоюється. У порівнянні з традиційною фолієвою кислотою, MEGNAFOLATE® структура ближче до екстракції з рослин. Дослідження показали, що MEGNAFOLATE® можуть бути безпосередньо поглиненілюдського організму незалежно від впливу різноманітності генів ферментів, що метаболізують фолат. Тому препарати, що містять МЕГНАФОЛАТ® буде better для вагітних жінок та їхніх дітей.
Зрештою, остаточне випробування має допомогти визначити найбезпечнішу та найефективнішу форму добавок фолієвої кислоти для вагітних жінок та їхніх дітей.
Література:
https://trialsjournal.biomedcentral.com/articles/10.1186/s13063-020-04320-3
Pietrzik K, Bailey L, Shane B. Фолієва кислота та 1-5-метилтетрагідрофолат:
порівняння клінічної фармакокінетики та фармакодинаміки. Clin Pharmacokinet. 2010;49(8):535–48.
Page R, Robichaud A, Arbuckle TE, Fraser WD, MacFarlane AJ. Загальний фолат і неметаболізована фолієва кислота в грудному молоці поперечного перерізу канадських жінок. Am J Clin Nutr. 2017;105(5):1101–9.
Houghton LA, Yang J, O’Connor DL. Неметаболізована фолієва кислота та загальні концентрації фолієвої кислоти в грудному молоці не піддаються впливу низьких доз фолієвої кислоти. Am J Clin Nutr. 2009; 89 (1): 216–20.
Дуглас Вілсон Р., Аудіберт Ф., Брок Дж. А., Керрол Дж., Картьє Л., Ганьон А. та ін. Фолієва кислота та полівітаміни до зачаття для первинної та вторинної профілактики дефектів нервової трубки та інших чутливих до фолієвої кислоти
вроджені аномалії. J Obstet Gynaecol Канада. 2015;37(6):534–49.
Verwei M, Arkbåge K, Mocking H, Havenaar R, Groten J. Зв'язування фолієвої кислоти та 5-метилтетрагідрофолату з білками, що зв'язують фолат, під час проходження шлунка відрізняється в динамічній моделі шлунково-кишкового тракту in vitro. J Nutr. 2004; 134(1):31–7.
Nygren-Babol L, Jägerstad M. Фолієзв'язуючий білок у молоці: огляд біохімії, фізіології та аналітичних методів. Crit Rev Food Sci Nutr. 2012;52(5):410–25.

 Español
Español Português
Português  русский
русский  Français
Français  日本語
日本語  Deutsch
Deutsch  tiếng Việt
tiếng Việt  Italiano
Italiano  Nederlands
Nederlands  ภาษาไทย
ภาษาไทย  Polski
Polski  한국어
한국어  Svenska
Svenska  magyar
magyar  Malay
Malay  বাংলা ভাষার
বাংলা ভাষার  Dansk
Dansk  Suomi
Suomi  हिन्दी
हिन्दी  Pilipino
Pilipino  Türkçe
Türkçe  Gaeilge
Gaeilge 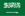 العربية
العربية  Indonesia
Indonesia  Norsk
Norsk  تمل
تمل  český
český  ελληνικά
ελληνικά  український
український  Javanese
Javanese  فارسی
فارسی  தமிழ்
தமிழ்  తెలుగు
తెలుగు  नेपाली
नेपाली  Burmese
Burmese  български
български  ລາວ
ລາວ  Latine
Latine  Қазақша
Қазақша  Euskal
Euskal  Azərbaycan
Azərbaycan  Slovenský jazyk
Slovenský jazyk  Македонски
Македонски  Lietuvos
Lietuvos  Eesti Keel
Eesti Keel  Română
Română  Slovenski
Slovenski  मराठी
मराठी  Srpski језик
Srpski језик 






 Online Service
Online Service